04008 § 8 MPG: Harmonisierte Normen, Gemeinsame Technische Spezifikationen
|
Das MPG wurde mit dem Geltungsbeginn der MDR aufgehoben. Allerdings hat es noch so lange Bedeutung, wie die sogenannten Legacy Devices verkehrsfähig sind. Denn die Legacy Devices entsprechen noch den alten Richtlinien 90/385/EWG oder 93/42/EWG und das MPG beinhaltet die nationalen Regeln für die Umsetzung der Richtlinien (s. Kap. 02120, 2.13). Deshalb stellen wir Ihnen die Kommentierung des MPG auch weiterhin in diesem Werk zur Verfügung.
Unter Mitarbeit von Frau Dr. Ing. Vera Sattelmayer, DIN, im Hinblick auf Normen und Harmonisierte Normen.
Arbeitshilfen: |
§ 8 Harmonisierte Normen, Gemeinsame Technische Spezifikationen
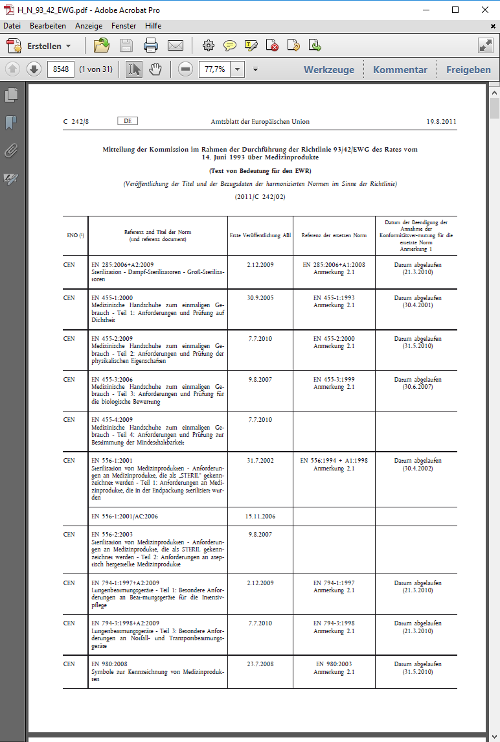
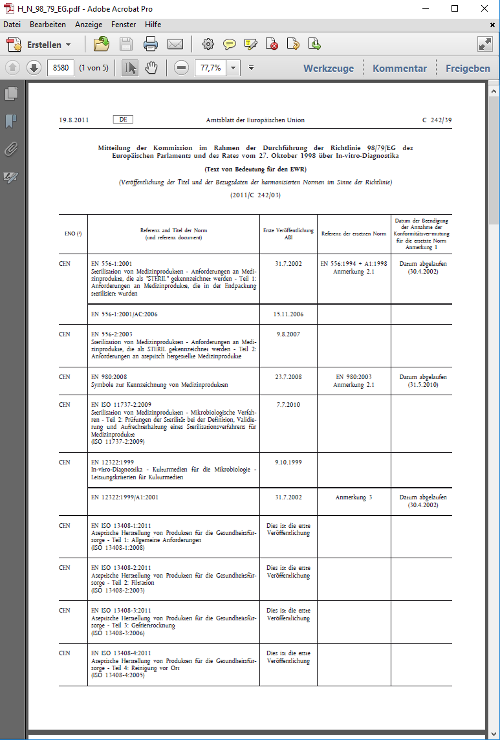
(1) Stimmen Medizinprodukte mit harmonisierten Normen oder ihnen gleichgestellten Mono-graphien des Europäischen Arzneibuches oder Gemeinsamen Technischen Spezifikationen, die das jeweilige Medizinprodukt betreffen, überein, wird insoweit vermutet, dass sie die Bestim-mungen dieses Gesetzes einhalten.
(2) Die Gemeinsamen Technischen Spezifikationen sind in der Regel einzuhalten. Kommt der Hersteller in hinreichend begründeten Fällen diesen Spezifikationen nicht nach, muss er Lösungen wählen, die dem Niveau der Spezifikationen zumindest gleichwertig sind. |
1 Einleitung
Mitte der achtziger Jahre vereinbarten die damaligen Staaten der Europäischen Gemeinschaft Maßnahmen zur Schaffung eines einheitlichen europäischen Binnenmarkts zur Sicherstellung des freien Warenverkehrs innerhalb der Gemeinschaft. Eine wesentliche flankierende Maßnahme zur Erreichung dieses Ziels war die Erarbeitung von Europäischen Normen durch die europäischen Normungsorganisationen unter dem Mandat der Europäischen Kommission in Brüssel. Festgelegt wurde eine eindeutige Trennung der Zuständigkeiten zwischen dem Europäischen Gesetzgeber und den europäischen Normungsorganisationen.
Die „Neue Konzeption” auf dem Gebiet der technischen Harmonisierung und der Normung (ABl. C 136 vom 4. Juni 1985) basierte auf folgenden Grundprinzipien: